Optimalizácia liečby imúnnej trombocytopénie a nové stratégie liečby trombocytopénie pri aplastickej anémii a myelodysplastickom syndróme
Na tohtoročnom kongrese EHA odzneli viaceré prednášky na tému imúnnej trombocytopénie (ITP), jej patofyziológie, nových možností a optimalizácie jej liečby. ITP je získané krvácavé ochorenie podmienené zvýšenou deštrukciou trombocytov (Tr) spôsobenou autoprotilátkami proti Tr. V patogenéze choroby sa uplatňuje dysregulácia T-lymfocytov (T-Ly), abnormality T-helperových buniek (Th1 a Th17) v dôsledku poruchy regulačných T-Ly (Treg), ale aj aktivácia cytotoxických T-Ly. Pacienti s ITP majú v cirkulácii zvýšený počet B-Ly produkujúcich protilátky anti- GPIb/IIIa príp. GPI/IX/V a pri deštrukcii trombocytov s naviazanými protilátkami zohrávajú úlohu Fc receptory makrofágov (FCγRII a FCγRIII) sleziny a pečene. Dnes je však známe, že pri ITP sa uplatňuje aj porucha trombopoézy, t. j. protilátkami sprostredkovaná porucha maturácie megakaryocytov a znížená produkcia trombocytov1 (obrázok 1). Lepšie poznanie patofyziológie ITP otvára aj nové možnosti jej liečby. Okrem tradičnej imunosupresívnej liečby kortikoidmi, splenektómie, imunomodulačnej liečby iv. imunoglobulínmi (IVIg) sa využívajú anti-CD 20 protilátky (rituximab) na supresiu B-Ly a v poslednom desaťročí sa sľubnou javí najmä „fyziologická liečba“, ktorú predstavujú agonisty receptorov pre trombopoetín (TPO-RA), ako je romiplostim a eltrombopag.
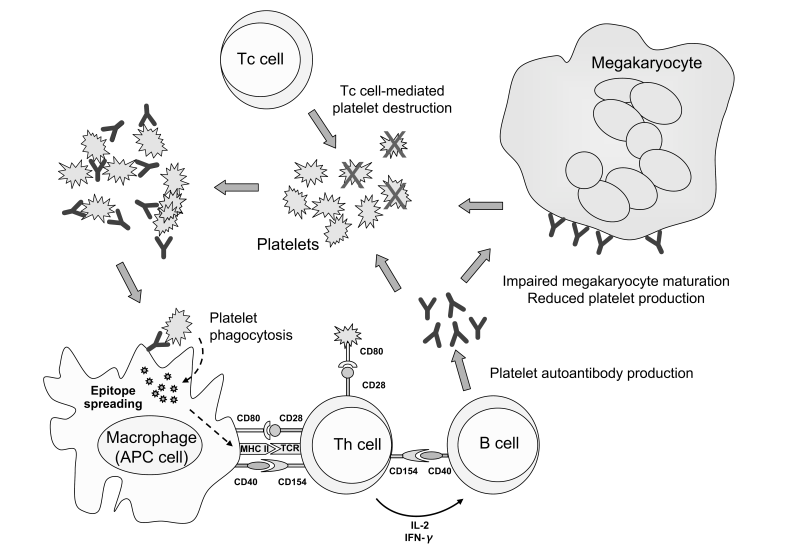
Obrázok 1: Patofyziologické mechanizmy pri vzniku ITP a ich vplyv na reguláciu trombocytov (podľa Stasi, R., 2011)
James Bussel z New Yorku, svetovo uznávaný expert na ITP, predniesol komplexnú edukačnú prednášku o ITP a najnovších možnostiach liečby. Podľa súčasných odporúčaní pre manažment ITP2, 3 sa za konvenčnú liečbu novodiagnostikovanej ITP považuje kortikoterapia (s iniciálnou odpoveďou 70 – 80 %, ale trvalou remisiou len v 10 – 30 %), IVIg na rýchle zvýšenie Tr v urgentných situáciách (zvyčajne prechodný efekt v 70 – 80 %) a anti-D imunoglobulín (efekt 50 – 70 %). Za liečbu druhej línie sa považuje splenektómia, po ktorej sa pozoruje dlhodobá remisia bez relapsov až v 65 % pacientov, ak sa vykoná do 12 mesiacov od diagnózy ITP. Rituximab vedie k remisii približne v 40 % pacientov, ale len v 20 % k trvalej remisii. Po zlyhaní liečby v 1. a 2. línii sa odporúčajú lieky s neurčitým efektom (danazol, cyklosporín A, mykofenolát, azatioprin, vinca alkaloidy), pričom do tejto línie boli pôvodne zaradené aj najnovšie lieky, agonisty TPR-R (romiplostim a eltrombopag). Bussel prezentoval súčasnú stratégiu liečby pri novodiagnostikovanej ITP, perzistujúcej ITP (trvanie 3 – 12 mesiacov) a chronickej ITP (trvanie > 12 mesiacov) podľa najnovšej práce Coopera z roku 20174 (obrázok 2).
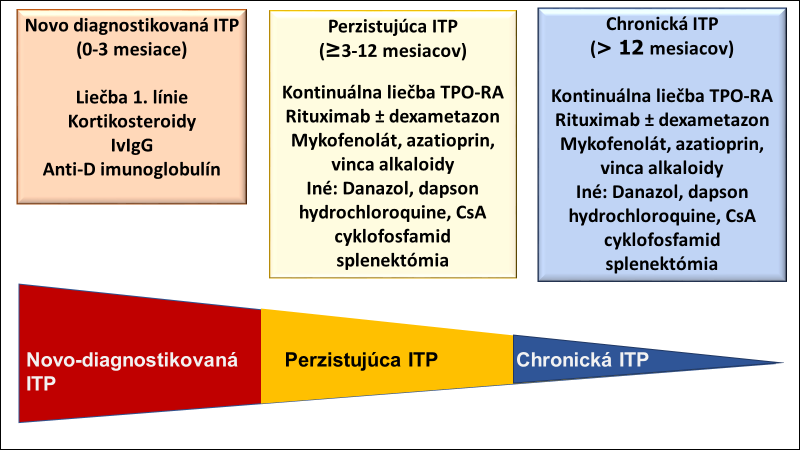
Obrázok 2: Súčasná stratégia liečby pacientov s primárnou ITP (podľa Cooper, N., BJH 2017)
IvIgG – intravenózny imunoglobulín, TPP-RA – antagonisty trombopoetínového receptora, CsA – cyklosporín A
S ohľadom na benefity a možné riziká konvenčnej liečby ITP sa v dnešnej ére dostupnosti TPO-R agonistov mení pohľad na stratifikáciu liečebných línií ITP a agonisty TPO-R (TPO-RA) sa dostávajú do druhej línie liečby ITP.4 V súčasnosti sú registrované dva TPO-RA : Eltrombopag, nepeptidová malá molekula, ktorá sa viaže na TPO-R v mieste jeho transmembránovej domény a aktivuje intracelulárne cesty JAK-STAT a MAPK na zvýšenie produkcie trombocytov. Romiplostim je trombopoézu stimulujúca „peptibody“, rekombinantný fúzny proteín pozostávajúci z dvoch konštantných častí (Fc fragmenty) pripojených na peptidovú doménu obsahujúcu 4 väzobné miesta pre TPO-R. Bussel prezentoval publikované údaje o odpovedi dospelých jedincov s ITP (vzostup Tr > 50 × 109/l) na liečbu s TPO-RA, pozorované v dvoch multicentrických randomizovaných kontrolovaných štúdiách. V prvej štúdii s. c. 52-týždňová aplikácia romiplostinu v dávke 3 – 10 μg týždenne viedla k odpovedi počas trvania liečby až v 71 – 92 % oproti 25 – 51 % pacientov liečených štandardnou liečbou.5 V 6-mesačnej štúdii s aplikáciou 50 mg eltrombopagu p. o. pretrvávala odpoveď počas liečby v 79 vs 28 % pacientov užívajúcich placebo (p < 0,0001).6 V nedávnej štúdii, ktorá sledovala počet trombocytov po vysadení eltrombopagu, sa kompletná remisia (KR) pozorovala počas viac ako 110 týždňov v 50 % pacientov, v prípade relapsu po prerušení eltrombopagu priaznivo odpovedalo na opätovnú liečbu 11/12 pacientov.7 Liečba TPO-RA vedie k vzostupu trombocytov a redukcii krvácavých prejavov a tieto lieky sa dnes považujú za účinné a bezpečné na liečbu chronickej ITP s vysokým rizikom krvácania po zlyhaní liečby prvej línie. Kombinácia vysokodávkovaného dexametazónu (40 mg p. o., D1-4) a eltrombopagu (50 mg, D5-32) u 12 pacientov s novodiagnostikovanou ITP viedla k trvajúcej remisii v 6. mesiaci (Tr > 100 × 109/l) v 50 % pacientov, ďalších 25 % pacientov malo počet Tr > 30 × 109/l.8 Aditívny efekt môže mať aj kombinácia rituximabu (1 cyklus) a dexametazónu (3 cykly 3- až 4-dňovej liečby dexametazónom), dobrý kuratívny efekt tejto kombinácie sa pozoroval u dospelých a žien s ITP počas 1 – 2 rokov od diagnózy ITP, ale nie v iných skupinách pacientov.9
Syk inhibítor (fosfamatinib) predstavuje nový nádejný liek na liečbu refraktérnej ITP. Syk (spleen tyrosine kinase) je cytoplazmatický enzým, ktorý sa spája s Fcγ receptorom zápalových buniek a aktiváciou signálnych ciest iniciuje zápalovú odpoveď. Inhibícia Syk môže viesť k zníženiu deštrukcie cirkulujúcich s protilátkou viazaných trombocytov, ktorá sa uskutočňuje cez FcγR makrofágy v slezine a v pečeni. Pilotná štúdia so Syk inhibítorom R788 potvrdila vzostup počtu Tr ≥ 50 % u dospelých pacientov s refraktérnou ITP.10
James Bussel z New Yorku predniesol aj ďalšiu komplexnú prednášku, v ktorej prezentoval úvahy o možnostiach dlhodobej liečby ITP agonistami TPO-R. Tieto lieky sa zvyčajne považujú za premosťujúcu a udržiavaciu liečbu. Vzhľadom na často neustupujúci priebeh chronickej ITP sa uvažuje o prolongovanej liečbe s TPO-RA, trvajúcej mesiace, prípadne roky, preto je dôležité poznať ich účinnosť a bezpečnosť pri dlhodobej liečbe, ako aj manažment liečby na zaistenie optimálneho efektu. Otázkou je dĺžka liečby, spôsob ukončenia liečby pri trvajúcej odpovedi a predpoveď priebehu choroby po ukončení liečby. Štúdia EXTEND, ktorá sledovala efekt prolongovanej liečby u 301 pacientov liečených ≥ 1 rok až ≥ 6 rokov, potvrdila rýchly vzostup počtu Tr do 2 týždňov po začatí liečby a kontinuálnu odpoveď Tr > 50 × 109/l počas viac ako 31 týždňov vo viac ako 50 % pacientov.11 Vedľajšie účinky boli prevažne mierne, najčastejšie bolesti hlavy, zvýšenie ALT, nazofaryngitída, katarakta. Zvýšenie ALT a trombotické príhody sa vyskytli najčastejšie v prvom roku liečby. Incidencia trombotických príhod v 6 štúdiách s eltrombopagom bola 0 – 6,7 % a v 8 štúdiách s romiplostimom 0 – 6,5 %. Riziko trombózy u pacientov s ITP okrem štandardných rizikových faktorov vrátane komorbidít vyššieho veku môže zvyšovať aj liečba ITP (kortikosteroidy, splenektómia, IVIG, TPO-RA). U pacientov liečených eltrombopagom počas 2 rokov sa nepozorovalo klinicky relevantné zvýšenie depozitov retikulínu alebo kolagénu v kostnej dreni.11 Pretrvávanie efektu po vysadení TPO-RA sledovali dve štúdie. V štúdii Gonzalez-Lopeza a kol. pretrvávala remisia po ukončení liečby eltrombopagom bez potreby ďalšej terapie až u 26/46 (56,5 %) pacientov s mediánom 9 (rozptyl 6 – 25) mesiacov.7 V štúdii s romiplostimom si zo 75 pacientov s primárnou ITP trvajúcou ≤ 6 mesiacov a liečených 12 mesiacov romiplostimom po vysadení liečby udržalo remisiu 24 (32 %) pacientov.12 V prospektívnej štúdii zahŕňajúcej 32 pacientov liečených eltrombopagom v dávke 75 mg najmenej 4 mesiace Bussel a spol. (2015) sledovali pomalé taperovanie liečby do 2 rokov. U pacientov s počtom Tr > 50 × 109/l sa znižovala dávka o 10 – 20 % v 4-týždňovom intervale. Na liečbu odpovedalo celkom 20 pacientov, u 10 pacientov bolo možné v priebehu 2 rokov liečbu vysadiť. 8/10 respondentov si udržalo Tr > 50 × 109/l dlhšie ako 1 rok po ukončení liečby. U ďalších 10 respondentov v čase ukončenia štúdie ešte pokračovalo postupné znižovanie dávky, zatiaľ bez ukončenia liečby.13
Bussel na záver upozornil na úskalia použitia TPO-RA u pacientov s ITP: 1) nemožnosť predvídania odpovede (koho liečiť, iniciálna dávka?), 2) efekt liečby nie je okamžitý (zvyčajne do 2 týždňov), 3) nie je jasné, kedy sa má liečba ukončiť a zmeniť na inú terapiu, 4) nejasné pravidlá pre optimálny čas a spôsob taperovania liečby u pacientov v dobrom stave.
Aj v posterovej sekcii boli prezentované viaceré práce potvrdzujúce účinnosť a bezpečnosť TPO-RA v liečbe ITP. Ghanima (Abstrakt E1435) prezentoval zaujímavé údaje z registra pacientov s chronickou ITP severských krajín Európy (Nórsko, Dánsko, Švédsko). Z počtu 3 749 evidovaných pacientov s mediánom veku 56 rokov malo vstupný počet Tr < 50 × 109/l 24 %, anamnézu splenektómie 16 % a ≥ 1 typ predošlej liečby 41 % pacientov. Mitrovic a spol. (Abstrakt 1448) retrospektívne analyzovali efekt splenektómie u 130 pacientov s ITP a hodnotili prediktívne faktory na dosiahnutie remisie. Odpoveď dosiahlo až 117 (87,5 %) pacientov, 105 (79 %) KR a 12 (7,5 %) PR. Multivariačná analýza ukázala, že pre úspech splenektómie má prediktívny význam splenický typ deštrukcie, počet Tr > 47 × 109/l v deň operácie a počet Tr > 300 × 109/l na 7. deň po splenektómii. Relaps vznikol u 29/117 (24,8 %) pacientov, v tejto skupine bol signifikantne vyšší počet pacientov > 60 rokov a pacienti mali nižší počet Tr v 3. mesiaci po splenektómii oproti pacientom s KR (130 × 109/l vs 278 × 109/l).
Dve zaujímavé prednášky sa zaoberali možnosťou použitia TPO-TA pri iných diagnózach, ako je ITP, ktoré sú tiež spojené s klinicky závažnou trombocytopéniou.
P. Scheinberg zo Sao Paula prezentoval pokroky liečby pacientov s aplastickou anémiou (SAA), pri ktorej dochádza k imunologicky sprostredkovanému poškodeniu hematopoetických kmeňových buniek (HSC) a deštrukcii kostnej drene a pancytopénii v periférnej krvi. Pri SAA sa pozoruje oligoklonálna expanzia T-buniek, aktivácia Th1, zníženie Treg a zvýšený pomer Tg17/Treg. U pacientov so SAA sú signifikantne zvýšené hladiny trombopoetínu. TPO-R je prítomný aj na hemopoetických kmeňových bunkách (HSC). In vitro štúdie demonštrovali, že TPO zvyšuje expanziu HSC. Liečbou prvej voľby SAA je transplantácia HSC a imunosupresívna liečba, pre zlepšenie prežívania však ostáva kľúčovou suportívna liečba pri komplikáciách vyplývajúcich z pancytopénie. Sľubnou liečbou pri SAA sa dnes javia TPO-RA. Olnes a spol. v r. 2012 publikovali priaznivý vplyv eltrombopagu na hemopoézu pri refraktérnej SAA.14 Desmond a spol. (2014) v štúdii zahrňujúcej 43 pacientov liečených eltrombopagom počas 3 – 13 mesiacov pozorovali remisiu u 17 (43 %) pacientov s trvajúcou troj- alebo dvojlíniovou úpravou hemopoézy bez potreby transfúzií s mediánom vzostupu počtu Tr o 39 × 109/l a hladiny hemoglobínu o 38 g/l (rozptyl 1,5 – 8,2g/l).15 V najnovšej štúdii Townsley a spol. (2017) podávali 92 pacientom so SAA popri liečbe hATG (D1-4) a CsA (6 mesiacov) aj eltrombopag 150 mg v troch ramenách: 1) D14 – 6 mesiacov, 2) D14 – 3 mesiace a 3) D1 – 6 mesiacov. Celková odpoveď v 3. mesiaci bola 80 % (KR 30 % a PR 50 %) a v 6. mesiaci 87 % (KR 39 % a PR 48 %) s najvyšším zastúpením odpovedí v 3. skupine pacientov užívajúcich eltrombopag 6 mesiacov od 1. dňa liečby.16 Na základe pozorovaní ďalších štúdií P. Scheinberg prezentoval dávkovanie eltrombopagu pri SAA. Štandardne sa začína dávkou 50 mg s možným vzostupom na 150 mg denne, nižšia iniciálna dávka (25 mg) je potrebná u jedincov východnej Ázie a pacientov s hepatopatiou. Po dosiahnutí počtu Tr 150 – 250 × 109/l sa dávka zníži o 50 mg, pri stabilizovanom počte počas 2 týždňov je možné ďalšie postupné znižovanie. Pri počte Tr ≥ 250 × 109/l sa užívanie preruší na 1 týždeň, ak počet Tr klesne na < 100 × 109/l, liečba sa obnoví v dávke redukovanej o 50 mg. Pri stabilnej odpovedi trvajúcej 8 týždňov sa užívanie eltrombopagu vysadí. Liečba SAA eltrombopagom je potvrdená FDA od roku 2014 a EMA od roku 2015. Doterajšie výsledky ukázali, že liek môže užitočný už v l. línii liečby SAA. Súčasná randomizovaná štúdia RACE porovnáva prvolíniovú štandardnú liečbou SAA kombinácou hATG + CsA + steroidy s liečbu hATG + CsA + steroidy + eltrombopag od D14 počas 3 mesiacov.
M. Mittelman z Univerzitnej nemocnice v Tel Avive prezentoval možnosti zlepšenia suportívnej liečby myelodysplastického syndrómu (MDS) s použitím TPO-RA. MDS predstavuje rôznorodú skupinu klonálnych ochorení kostnej drene, sprevádzanú ťažkou pancytopéniou a závislosťou od transfúzií erytrocytov a trombocytov. Prežívanie a kvalita života pacientov závisí aj od kvality suportívnej liečby. Randomizovaná kontrolovaná štúdia s použitím romiplostimu u 71 pacientov s MDS ukázala signifikantne vyšší počet pacientov s odpoveďou počtu Tr (p < 0,001) a nižšími požiadavkami na transfúzie Tr (p < 0,001) oproti placebovej skupine. Medzi obomi skupinami nebol rozdiel v počte úmrtí a prechodu do akútnej myeloickej leukémie17 (AML). ASPIRE je placebom kontrolovaná štúdia, zameraná na efekt liečby eltrombopagom v dávke 100 mg u pacientov s MDS a AML. V 1. časti (8 týždňov) sa potvrdil vzostup počtu Tr u 4/17 pacientov s redukciou potreby transfúzií Tr u 10/17 pacientov. Z vedľajších účinkov sa vyskytla elevácia ALT, bezo zmien v blastickej infiltrácii kostnej drene. 2. časť štúdie (12 týždňov) potvrdila nižší výskyt klinicky relevantných trombocytopenických príhod v skupine liečenej eltrombopagom (54 %) oproti placebu (69 %); p = 0,031. Teraz prebieha 3. časť tejto štúdie (Extension).18 V súčasnosti beží aj ďalšia prospektívna, placebom kontrolovaná štúdia s použitím eltrombopagu v dávke 50 –300 mg denne počas ≥ 6 mesiacov.19 Predbežné výsledky ukázali priaznivú odpoveď v počte Tr u 28/59 (47 %) pacientov oproti placebu (1/31; 3 %) bez zvýšenia progresie choroby do AML. U niektorých pacientov sa pozorovala aj erytroidná a neutrofilná odpoveď. Výsledok liečby MDS eltrombopagom nie je ovplyvnený vekom, pohlavím, trvaním MDS, WHO klasifikáciou ani cytogenetickým nálezom. Štúdia SUPPORT je randomizovaná, dvojito zaslepená, placebom kontrolovaná štúdia u dospelých pacientov s MDS, v ktorej sa v liečebnej skupine podáva eltrombopag 200 mg denne v kombinácii s azacitidínom v dávke 75 mg/m2.20 Výsledky týchto štúdií prispejú k novým poznatkom o nových možnostiach liečby pacientov s takým vážnym ochorením, akým je myelodysplastický syndróm.
Prof. MUDr. Angelika Bátorová, PhD.
Klinika hematológie a transfúziológie LFUK, SZU, Univerzitná nemocnica, Bratislava
E-mail: batorova(at)hotmail.sk
Literatúra
1. Stasi, R. Pathophysiology and therapeutic options in primary immune thrombo¬cytopenia. Blood Transfus 2011;9: 262 – 273.
2. Provan, D., et al. International consensus report on the inves¬tigation and management of primary immune thrombocytopenia. Blood. 2010; 115: 168 – 175.
3. Neunert, C. et al. The American Society of Hematology 2011 evidence-based practice guideline for immune thrombocytopenia. Blood 2011;117: 4190 – 4207.
4. Cooper, N. State of the art – how I manage immune thrombcytopenia. Br J Haematol 2017; 177: 39–54. doi:10.1111/bjh.14515.
5. Kuter, D. J. et al. Romiplostim or standard care in patients with immune thrombocytopenia. N Engl J Med 363: 1889 – 1899.
6. Cheng, G. et al. Eltrombopag for management of chronic immune thrombocytopenia (RAISE): a 6-month, randomised, phase 3 study. Lancet 2011;377: 393 – 402.
7. González-Lopez, T. J. et al. Successful discontinuation of eltrombopag after complete remission in patients with primary immune thrombocytopenia.Am J Hematol 2015:90:E40-E43.
8. Gomez-Almaguer, .D, et al. Eltrombopag and high-dose dexamethasone as frontline treatment of newly diagnosed immune thrombocytopenia in adults. Blood 2014;123: 3906 – 3908.
9. Chapin, J. et al. Gender and duration of disease differentiate responses to rituximab-dexamethasone therapy in adults with immune thrombocytopenia.Am J Hematol 2016;91: 907 – 911.
10. Podolanczuk, A. et al. Of mice and men: an open-label pilot study for treatment of immune thrombocytopenic pur¬pura by an inhibitor of Syk. Blood. 2009;113: 3154 – 3160.
11. Bussel, J. et al. Haematologica 2016;101 (S1) abst. S517, oral presentation EHA 2016
12. Newland A, et al. Remission and platelet responses with romiplostim in primary immune thrombocytopenia: final results from a phase 2 study. Br J Haematol 2016; 172,2: 262 – 273.
13. Bussel, J. et al. Blood 2015;126: Abstract 1054.
14. Olnes, M. J. K. et al. Eltrombopag and improved hematopoiesis in refractory aplastic anemia. N Eng J Med 2012;367: 11 – 19.
15. Desmond, R. et al. Eltrombopag restores trilineage hematpoiesis in refractory severe aplastic anemia thac can be sustained on discontinuation of drug. Blood 2014;123,12: 1818 – 1825.
16. Townsley, D. M. et al. Eltrombopag Added to Standard Immunosuppression for Aplastic Anemia. N Engl J Med 2017; 376: 1540 – 1550.
17. Kantarjian, H. et al. Blood 2015; 126, Abstract 2863.
18. Komrjoki Use of eltrombopag for treatment of myelodysplastic syndromes. Lancet Haematol 2017; 4, 3: e99-e100.
19. Oliva EN, et al. Eltrombopag versus placebo for low-risk myelodysplastic syndromes with thrombocytopenia (EQoL-MDS): phase 1 results of a single-blind, randomised, controlled, phase 2 superiority trial. Lancet Haematol 2017;4:e127-e136.
20. Dickinson, M. et al. Blood 2016; 128; Abstract 163.